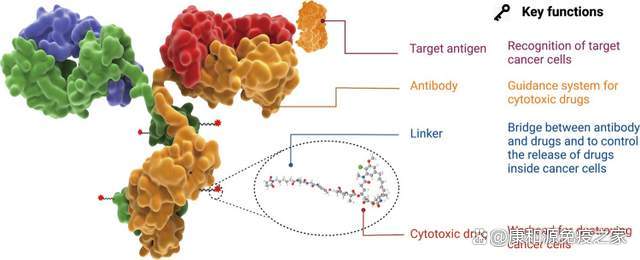
抗體-藥物偶聯物 (ADC) 是一類快速興起的癌症治療方式,夠選擇性地將高細胞毒性有效載荷遞送至腫瘤。ADC由抗體、細胞毒載荷和化學連接體組成。這類藥物就像一枚精確制導的“生物導彈”,能夠准確摧毀癌細胞,改善治療窗口,減少脫靶副作用。
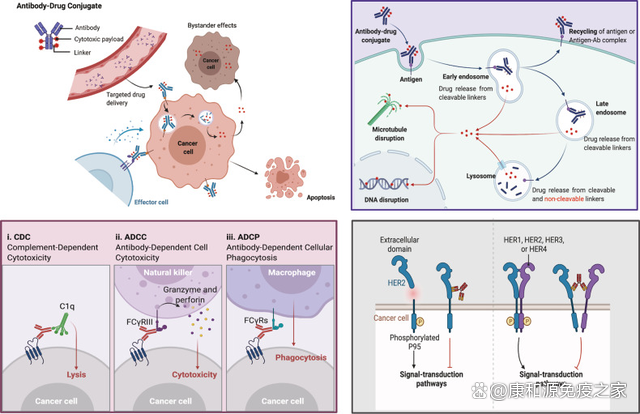
一旦ADC的單抗與癌細胞上特異性表達的靶抗原結合,ADC就會被細胞內吞/內化,形成早期內體,隨後成熟爲晚期內體,最後與溶酶體融合。細胞毒性載荷最終通過化學或酶介導的溶酶體釋放,通過靶向DNA或微管導致細胞凋亡或死亡當釋放的有效載荷具有滲透性或跨膜性時,還可能誘發旁觀者效應,從而增強ADC的療效。此外,這些藥物的旁觀者效應也可能改變腫瘤微環境,從而進一步增強adc的殺傷作用。
經過數十年的努力,目前有超過100種ADC藥物處于臨床開發階段。
新一代TROP-2 ADC藥物:SKB264
在2024年美國癌症研究協會(AACR)大會上我國原創的一款名爲“SKB264”的TROP-2抗體藥物偶聯物(ADC)以口頭報告形式,發表該藥用于經治晚期胃/胃食管結合部(G/GEJ)腺癌的Ⅱ期拓展研究結果,這是全球首個公布胃癌研究數據的TROP-2 ADC!
SKB264是靶向TROP2的人源化單克隆抗體、可酶促裂解的Linker和新型拓撲異構酶I抑制劑組合而成的新一代抗體偶聯藥物(ADC),結合了單抗對腫瘤細胞表面靶抗原的特異性和細胞毒性藥物的高效性,設計有獨特的連接子來連接有效負載,該連接子響應細胞外pH值及腫瘤細胞內的酶而發生裂解,促進腫瘤細胞內及腫瘤微環境內有效負載的有效釋放,從而發揮其抗腫瘤作用。
在KL264-01 II期臨床研究中,納入了48例胃或胃食管交界部(G/GEJ)腺癌患者,客觀緩解率(ORR)達22.0%,疾病控制率(DCR)達80.5%,中位無進展生存期(mPFS)爲3.7個月,中位總生存期(mOS)爲7.6個月,12個月總生存期(OS)率爲32.6%。
由此可見SKB264在胃或胃食管交界部(G/GEJ)腺癌的療效。
2023年第46屆美國聖安東尼奧乳腺癌研討會(SABCS)上公布了SKB264在局部晚期或轉移性三陰性乳腺癌(TNBC)患者的II期擴展研究。在59例局部晚期或轉移性TNBC治療患者中,客觀緩解率(ORR)爲42.4%,其中3例患者達到完全緩解(CR),疾病控制率(DCR)爲76.3%,中位緩解持續時間(mDoR)爲11.5個月。此外,中位無進展生存期(mPFS)爲5.7個月,中位總生存期(mOS)達到16.8個月,12個月和24個月總生存率(OS)分別爲65%和39.5%。在接受SKB264治療的研究中,近40%的患者在兩年內存活。在TROP2高表達患者亞組中,ORR爲53.1%,mDoR爲11.1個月,mPFS爲5.8個月,12個月和24個月OS率分別爲65.3%和57.3%。
HER2陰性乳腺癌ADC藥物Dato-DXd申請獲受理
在中國,乳腺癌是女性常見惡性腫瘤之一,發病率位居女性惡性腫瘤之首。有研究表明30%以上的人類腫瘤中存在HER2基因的擴增/過度表達(如乳腺癌、卵巢癌、子宮內膜癌、輸卵管癌、胃癌和前列腺癌等);其中20%-30%的原發性浸潤性乳腺癌有HER2基因的擴增/過度表達。
4月2日,datopotamab deruxtecan(Dato-DXd)的生物制品許可申請(BLA)已在美國受理,用于治療不可切除或轉移性激素受體(HR)陽性、HER2陰性的乳腺癌成人患者,這些患者既往接受過不可切除或轉移性疾病的全身治療。美國食品和藥物管理局(FDA)對其監管決定采取行動的日期是處方藥用戶費用法案日期,是在2025年第一季度。
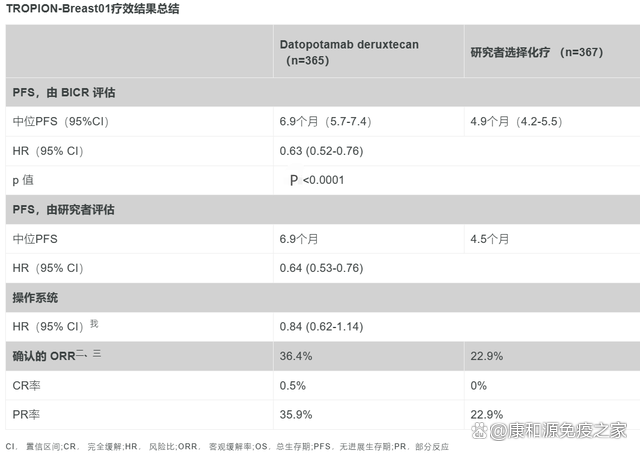
此次BLA得到了3期 TROPION-Breast01試驗(NCT05104866)結果的支持。根據2023年歐洲腫瘤內科學會年會上公布的數據,與研究者選擇的化療相比,Dato-DXd將疾病進展或死亡的風險降低了37%。Dato-DXd和化療的確認客觀緩解率(ORR)分別爲36.4%和22.9%。無進展生存期(PFS)研究結果在2023年聖安東尼奧乳腺癌研討會上公布。接受Dato-DXd治療的患者的中位無進展生存期(PFS)爲6.9個月,而接受化療的患者爲4.9個月。
研究表明,SKB264治療可能是一種很有前途的治療療法,有望爲胃癌、肺癌和乳腺癌患者提供臨床益處。隨著生物技術的不斷進步,相信不久的將來定能真正實現“魔法子彈”的設想。
免責聲明:康和源免疫之家爲免疫科普平台,文本參考來源于網絡,版權歸原作者所有。
該文章僅供分享,如涉嫌侵犯您的著作權請聯系我們刪除,謝謝!
參考資料
Frontiers | Preclinical profiles of SKB264, a novel anti-TROP2 antibody conjugated to topoisomerase inhibitor, demonstrated promising antitumor efficacy compared to IMMU-132 (frontiersin.org)