2024 年 4 月5日,美國食品藥品監督管理局(FDA) 批准了ciltacabtagene autoleucel (西達基奧侖賽) 用于治療既往接受過一種或多種治療的難治性或複發性多發性骨髓瘤。這種治療可用于對來那度胺無反應且先前接受過免疫調節劑和蛋白酶體抑制劑的患者。
美國食品藥品監督管理局(FDA)根據3期臨床試驗CARTITUDE-4的結果批准了該治療。該臨床試驗的結果已在2023年美國臨床腫瘤學會 (ASCO) 年會上公布。結果顯示:西達基奧侖賽組的無進展生存率爲75.9%,標准治療組爲48.6%;西達基奧侖賽組比標准治療組有更多的患者完全緩解或更好(73.1% vs 21.8%),總體緩解(部分緩解或更好)分別爲84.6%和67.3%,在有反應的患者中,西達基奧侖賽組估計有84.7%的患者持續至少12個月有反應,而標准治療組爲63.0%。

西達基奧侖賽是傳奇生物自主研發的一款具有兩種靶向B細胞成熟抗原(BCMA)單域抗體的嵌合抗原受體(CAR)T細胞免疫療法。
2022年2月,美國FDA正式批准西達基奧侖賽上市,用于治療複發/難治性多發性骨髓瘤(R/R MM)患者。這是全球第二款獲FDA批准的BCMA CAR-T,也是首款獲FDA批准的國産CAR-T細胞療法。

根據2023年歐洲血液學協會(EHA)大會上公布的1b/2期CARTITUDE-1研究(NCT03548207)的最終結果顯示:總緩解率(ORR)高達97.9%,其中包括82.5%的嚴格完全緩解(CR)患者。此外,12.4%的患者有非常好的部分緩解,3.1%的患者經曆了部分緩解(PR)。中位無進展生存期(PFS)爲34.9個月,中位緩解持續時間(DOR)爲33.9個月。
多發性骨髓瘤(Multiple myeloma, MM)是一種漿細胞惡性腫瘤,約占血液系統惡性腫瘤的10%。據統計,我國多發性骨髓瘤每年新發病例數高達27800例,作爲一種多發于老年人的惡性血液腫瘤,隨著我國人口老齡化的加速,多發性骨髓瘤的發病率也將逐年上升。多發性骨髓瘤目前仍無法治愈,多數多發性骨髓瘤患者會出現骨頭疼痛、骨折,約半數患者會出現腎髒損傷,甚至需要進行血液透析,嚴重影響患者生存。被稱爲“吃骨頭”的血液病。
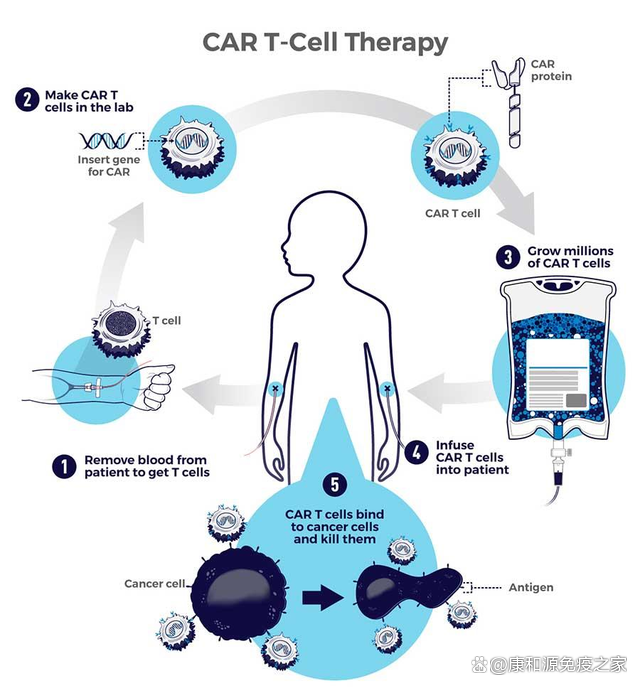
近年來熱門的CAR-T細胞療法,就是將病人自身免疫系統的T細胞提取出來,經過體外培養和改造,給這些T細胞裝備上特殊分子,使它們能識別並攻擊特定的靶細胞,再把改造過後的T細胞注射回病人身體,由這些T細胞來消滅靶細胞。
自體CAR-T産品:澤沃基奧侖賽
3月1日,國家藥品監督管理局正式下達通知,批准澤沃基奧侖賽注射液用于治療複發或難治性多發性骨髓瘤成人患者,既往經過至少3線治療後進展(至少使用過一種蛋白酶體抑制劑及免疫調節劑)。
澤沃基奧侖賽是一種針對BCMA的自體CAR-T産品,具有全人源 BCMA 特異性單鏈可變片段的CAR構建體,旨在具有更低的免疫原性和更高的穩定性。
此次獲批是基于一項在中國進行的開放標簽、單臂、多中心II期的臨床試驗(LUMMICAR STUDY 1,NCT03975907)。根據2022年美國血液學會(“ASH”)公布的試驗結果,澤沃基奧侖賽表現出令人鼓舞的療效和良好的安全性。從2019年7月23日開始,14名中位年齡爲54歲(範圍34,62歲)的患者接受了單次澤沃基奧侖賽輸注。截至數據截止日期(2023年7月17日),中位生存隨訪時間爲37.7個月。總緩解率爲100%,其中11例(78.6%)患者達到完全緩解(CR)或嚴格完全緩解(sCR),2例(14.3%)患者獲得了很好的部分緩解,1例(7.1%)患者獲得了部分緩解。所有達到CR或CR以上的患者微小殘留病竈(MRD)均爲陰性。所有患者的中位無進展生存期爲25.0個月,sCR/CR患者的中位無進展生存期爲26.9個月。

所有患者的中位緩解持續時間爲24.1個月,sCR/CR患者的中位緩解持續時間爲26.0個月。在數據截止時,5名受試者仍有持續的反應。

衆所周知CAR-T生産成本高,很難降價。但是這事被印度人做到了。
二三十萬的CAR-T産品—NexCAR19,緩解率達70%!
3月21日,《自然》期刊發布印度研發出一種經濟實惠的CAR-T細胞療法—NexCAR19,已獲中央藥品標准控制組織(CDSCO)批准震撼上市,用于治療血液癌症。該療法單次治療費用在3萬~4萬美元(約20萬~30萬人民幣)。

據了解,NexCAR19在患有不同形式淋巴瘤和白血病的成人中的早期臨床試驗表明,在接受治療的33人中,有19人在一個月的隨訪中腫瘤完全消失。另外四個人的腫瘤縮小了一半,總體緩解率爲70%。2023年12月在美國血液學會會議上公布的試驗結果顯示,兩項試驗中 67% 的患者(53人中有36人)的癌症程度顯著下降(客觀反應),大約一半的腫瘤完全消失(完全緩解)。
這無疑是一項重大的突破,大大降低了患者的經濟負擔,雖然對于普通民衆而言,NexCAR19的價格仍然不菲,但相較于百萬“天價”的CAR-T産品無疑是一項重大的突破!國內CAR-T價格高,多數是因爲原材料、耗材、設備等離不開進口,生産成本高。但是國內的CAR-T技術也在持續研究發展中,相信在多方努力下,這一療法能有更多降價的好消息傳來。
相信未來更多企業通過探索掌握這項技術後,價格也會降下來,惠及大多數患者。
免責聲明:康和源免疫之家爲免疫科普平台,文本參考來源于網絡,版權歸原作者所有。
該文章僅供分享,如涉嫌侵犯您的著作權請聯系我們刪除,謝謝!
參考資料
Cutting-edge CAR-T cancer therapy is now made in India — at one-tenth the cost (nature.com)
