本文來源:選自《中華內科雜志》, 2023,62(12) : 1394-1405.
摘要: 糖尿病腎髒病(DKD)是糖尿病主要慢性並發症之一,疾病負擔沉重。自《國家基層糖尿病防治管理指南(2018)》發布以來,隨著基層基本公共衛生服務和醫療能力的不斷提升、工作內容的不斷拓展,基層糖尿病防治管理工作需要細化的技術指南。本指南旨在推動基層DKD防治工作規範化,幫助基層醫生開展DKD的預防和控制,並對DKD患者進行綜合管理。主要內容包括管理基本要求、DKD概述、篩查、診斷與臨床分期、治療、患者隨訪及轉診。
本指南適用于≥18歲的T2DM。
糖尿病腎髒病概述
慢性腎髒病(chronic kidney disease,CKD)是由各種原因引起的慢性腎髒結構和功能障礙的總稱。糖尿病所致的腎髒損害稱爲DKD,其屬于CKD的範疇。DKD主要包括UACR≥30 mg/g 和/或估算的腎小球濾過率(estimated glomerular filtration rate,eGFR)<60 ml·min⁻1·1.73 m⁻2,且持續超過3個月。DKD是由慢性高血糖所致的腎損害,病變可累及全腎(包括腎小球、腎小管、腎間質及腎血管等),臨床上以持續性白蛋白尿和/或eGFR進行性下降爲主要特征,可進展爲終末期腎病(end stage renal disease,ESRD)。
糖尿病腎髒病篩查、診斷與臨床分期
一、篩查
推薦T2DM患者在確診糖尿病時篩查DKD,且以後每年至少篩查1次。篩查項目包括尿常規、UACR和血清肌酐(計算eGFR)。
二、診斷
DKD通常是根據UACR增高和/或eGFR下降,同時排除其他原因所導致的CKD而做出的臨床診斷。
推薦采用隨機尿測定UACR。UACR≥30 mg/g定義爲白蛋白尿,但僅單次UACR增高不能診斷爲白蛋白尿,需在3~6個月內重複檢測,3次中有2次UACR≥30 mg/g、排除感染等因素後方可診斷白蛋白尿。通常將UACR 30~300 mg/g稱爲微量白蛋白尿,UACR>300 mg/g稱爲大量白蛋白尿。診斷糖尿病白蛋白尿還需要排除其他的影響因素,如感染、發熱、24 h內運動、心力衰竭、女性月經期等均可能使UACR升高,結果分析時應考慮這些因素。若檢測24 h尿白蛋白定量,其診斷價值與UACR相當。
推薦檢測血清肌酐水平,並采用CKD-EPI公式計算eGFR(附錄4)。當糖尿病患者eGFR<60 ml·min-1·1.73 m-2可診斷爲eGFR下降。
當糖尿病患者UACR≥30 mg/g和/或eGFR<60 ml·min-1·1.73 m-2持續超過3個月,並排除其他原因所致的CKD時,臨床可以診斷爲DKD。
在臨床診斷DKD時需要注意:(1)明確糖尿病與慢性腎髒病之間的因果關系:應綜合考慮糖尿病病程、血糖控制情況、腎功能下降程度與速度以及是否合並其他微血管並發症等。典型的DKD臨床表現包括:病程較長的糖尿病、合並視網膜病變、出現白蛋白尿而無血尿,以及eGFR逐漸下降等。(2)關注UACR正常但eGFR下降,即正常白蛋白尿糖尿病腎髒病(normoalbuminuric diabetic kidney disease,NADKD)的患者。NADKD在高齡、女性及血糖控制良好的人群中較常見。(3)糖尿病視網膜病變(diabetic retinopathy,DR)是診斷DKD的重要依據之一。DR進展與腎髒病理改變及ESRD進展程度相關,DKD患者常常合並DR。
在診斷DKD時需排除其他病因所致的慢性腎髒病。當糖尿病患者伴有腎髒損害並出現以下任一情況時,需考慮非糖尿病腎髒病(nondiabetic kidney disease,NDKD)或DKD合並NDKD,並及時轉診至上級醫院明確病因:(1)出現活動性尿沉渣(紅細胞、白細胞、細胞管型等);(2)eGFR迅速下降;(3)UACR迅速增高或出現腎病綜合征;(4)給予血管緊張素轉化酶抑制劑(angiotensin- converting enzyme inhibitors,ACEI)或血管緊張素受體拮抗劑(angiotensin receptor blocker,ARB)治療後3個月內eGFR下降大于30%;(5)腎髒超聲檢查發現異常;(6)頑固性高血壓;(7)合並其他系統性疾病的症狀或體征等。
上述DKD的診斷及鑒別診斷是依據臨床表現及實驗室檢查而做出的臨床診斷,糖尿病合並腎損害的病因難以鑒別時,可行腎穿刺病理檢查。
三、臨床分期
確診DKD後,應聯合CKD分期(G1~G5)和白蛋白尿分期(A1~A3)判定DKD嚴重程度、進展和死亡風險及臨床隨訪和轉診頻率(表1)。例如,某DKD患者的eGFR爲40 ml·min-1·1.73 m-2、UACR爲358 mg/g,診斷爲DKD G3bA3,對應的DKD進展風險爲極高風險,應每年至少隨訪3次。
表1 根據eGFR和UACR分類的CKD進展風險及臨床隨訪和轉診頻率

注:eGFR爲估算的腎小球濾過率;UACR爲尿白蛋白/肌酐比值;CKD爲慢性腎髒病;背景顔色代表CKD進展和死亡的風險,表格中的數字爲建議每年隨訪的次數:綠色爲低風險,建議每年隨訪1次;黃色爲中風險,建議每年隨訪1次;橙色爲高風險,建議每年隨訪2次;紅色和深紅色爲極高風險,紅色建議每年隨訪3次,深紅色建議每年隨訪4次及以上;“如有CKD”表示雖無白蛋白尿,但可能存在其他腎髒損傷如病理、尿液、血液或影像學檢查異常;a爲轉診至腎髒專科隨訪的頻率
糖尿病腎髒病治療
一、治療目標
DKD的治療重在早期幹預,綜合管理,以減少蛋白尿,延緩eGFR下降,改善腎髒不良結局(如ESRD、腎髒相關死亡等)。科學、合理的治療策略包括生活方式幹預,血糖、血壓、血脂和體重的控制(表2)。

DKD患者的血糖控制應遵循個體化原則,根據患者年齡、病程、預期壽命、合並症、並發症、低血糖風險等,制定個體化控制目標(圖1)。

注:CKD爲慢性腎髒病;G1期爲eGFR≥90 ml·min -1·1.73 m -2,G5期爲eGFR<15 ml·min -1·1.73 m -2;大多數成年DKD患者HbA 1c控制目標爲7%,對于年齡輕、病程短、預期壽命長、低血糖風險小、無或合並輕度並發症、合並症少的DKD患者HbA 1c控制目標可進一步嚴格至<6.5%,其前提是無低血糖等不良反應;年齡大、病程長、預期壽命短、低血糖風險大、並發症嚴重、合並症多的DKD患者HbA 1c控制目標可放寬至8%
▲圖1 糖尿病腎髒病(DKD)患者糖化血紅蛋白(HbA1c)分層控制目標
DKD患者血壓控制目標在130/80 mmHg(1 mmHg=0.133 kPa)以下,舒張壓不宜低于60 mmHg,並應根據並發症及耐受情況設定個體化的血壓目標。
DKD患者的調脂和體重管理綜合控制目標同一般T2DM患者。
二、生活方式幹預
(一)營養幹預
1.總體原則:合理控制總熱量,達到或維持理想體重。合理選擇搭配食物,盡量做到營養均衡,食物多樣,滿足患者對各種營養素的需求。適當增加蔬菜和低血糖生成指數(glycemic index,GI)水果的攝入,選擇蛋類、奶類、水産類、禽畜類以及大豆及其制品等富含優質蛋白的食物,減少精制碳水化合物(如白米飯、面食等)及含糖飲料和加工肉類的攝入。eGFR<60 ml·min-1·1.73 m-2同時合並UACR≥30 mg/g或者eGFR<45 ml·min-1·1.73 m-2的患者盡量選用優質蛋白來源的食物。提倡選擇低GI的食物/品。選擇小份食物有助于增加食物種類。平均每天攝入食物種類數在12種以上,每周在25種以上。推薦營養攝入見表3。

2.蛋白質攝入:對于未進行透析治療的DKD患者,推薦的蛋白質攝入量爲0.8 g·kg-1·d-1,優質蛋白的比例應占50%以上;而透析患者常存在營養不良,可適當增加蛋白質攝入量至1.0~1.2 g·kg-1·d-1。優質蛋白來源的食物包括:雞蛋、牛奶、魚肉、蝦肉、雞肉、鴨肉、瘦牛肉、瘦羊肉、瘦豬肉、大豆等。
3.脂肪攝入:脂肪攝入需滿足人體對必需脂肪酸的需求,同時適當提高ω-3脂肪酸(如魚油等)的比例,有助于改善血脂代謝異常。
4.鈉、鉀攝入:每日的鈉攝入量應低于2 g(相當于5 g食鹽)。高鈉和低鈉飲食均可能增加高血壓、ESRD、心血管疾病(cardiovascular disease,CVD)及死亡風險。嚴重的DKD患者會出現血鉀失衡,高鉀血症(血鉀>5.5 mmol/L)及低鉀血症(血鉀<3.5 mmol/L)均會誘發心血管事件。對于合並高鉀/低鉀血症的DKD患者,應調控富含鉀的食材的攝入(表4)。

(二)運動幹預
適量規律運動有助于糖尿病患者的血糖、血壓和血脂控制,改善心、肺、腎以及認知功能,因此適當強度的運動可延緩DKD進展,同時減少DKD患者的CVD及死亡風險。
1.運動原則:運動目標應綜合考慮患者的年齡、心血管合並症、基礎運動水平、防跌倒能力等因素。運動可以從低強度、小運動量開始,並定期監測腎功能、電解質及尿蛋白等。
2.運動頻率:推薦每周進行150 min的中等強度運動,推薦每周至少活動3 d,連續不運動的天數不超過2 d(如每周5次、每次30 min)。根據患者的具體情況制定目標心率(target heart rate,THR),計算公式見附錄5。
3.運動類型:包括有氧運動、抗阻運動以及柔韌性訓練等。有氧運動包括健步走、乒乓球、太極拳、羽毛球、騎車和遊泳等。常見的抗阻運動項目則包括仰臥起坐、俯臥撐、擡舉啞鈴、拉伸拉力器等。柔韌性訓練(如伸展、拉伸等)在運動的准備階段和結束階段進行,多與有氧運動相結合。
4.運動禁忌:如有下列情況應禁止運動訓練:糖尿病酮症酸中毒;空腹血糖>16.7 mmol/L或血糖<3.9 mmol/L;糖尿病合並增殖性視網膜病變,嚴重的腎髒病,嚴重的心腦血管疾病(不穩定性心絞痛、嚴重心律失常、短暫性腦缺血發作);糖尿病合並急性感染等。
(三)體重管理
超重和肥胖可增加糖尿病患者的腎髒病風險,有效的體重管理是預防和治療DKD的重要輔助手段。超重爲體重指數(body mass index,BMI)介于24~<28 kg/m2,肥胖爲BMI≥28 kg/m2。BMI計算公式爲:BMI=體重(kg)÷身高2(m2)。建議超重和肥胖患者短期減重的目標是3~6個月減輕體重的5%~10%;長期(如1年)減重的目標爲BMI達到或接近24 kg/m2,或體重至少下降7%,並使體重長期維持在健康水平。超重或肥胖DKD患者的體重管理措施包括生活方式幹預、藥物治療及代謝手術等。
(四)戒煙戒酒
吸煙、飲酒是DKD進展的重要危險因素。DKD患者需做到戒煙戒酒,規律作息,配合診治。
三、降糖治療
(一)藥物治療原則
基層醫療機構應根據患者的具體病情制定治療方案,並指導患者使用藥物,同時充分評估患者心腎功能、並發症、合並症情況,根據eGFR調整藥物劑量;盡量避免使用低血糖風險較高的口服降糖藥物。不同腎功能分期降糖藥物的使用見附錄6。各類降糖藥物綜合獲益、風險評估表見附錄7。建議優先選擇具有腎髒獲益證據的藥物。
(二)具有腎髒獲益證據的降糖藥物
1.鈉-葡萄糖共轉運蛋白2抑制劑(sodium-glucose cotransporter 2 inhibitor,SGLT2i):SGLT2i通過抑制腎髒對葡萄糖的重吸收,促進尿糖排出,從而降低血糖。除此之外,部分SGLT2i還有降低白蛋白尿、延緩腎功能下降、並具有心血管保護作用。推薦在eGFR≥45 ml·min-1·1.73 m-2的DKD患者中使用SGLT2i。近期研究結果表明,部分SGLT2i可以在eGFR≥20 ml·min-1·1.73 m-2時使用。具體藥物適應證和禁忌證見藥品說明書。
SGLT2i的常見不良反應爲泌尿系統和生殖系統感染及血容量不足(如症狀性低血壓、頭暈、脫水)等,建議適當補水。同時應關注嚴重不良反應,如酮症酸中毒。
2.胰高糖素樣肽-1受體激動劑(glucagon like peptide-1 receptor agonist,GLP-1RA):GLP-1RA通過激活胰高糖素樣肽-1受體促進胰島素分泌、抑制胰高糖素分泌,從而降低血糖,並具延緩胃排空、抑制食欲等作用。部分GLP-1RA具有腎髒保護作用。GLP-1RA不應與二肽基肽酶Ⅳ抑制劑(dipeptidyl peptidase Ⅳ inhibitor,DPP-4i)聯合使用。GLP-1RA常見不良反應爲胃腸道反應。GLP-1RA禁用于有甲狀腺髓樣癌病史或家族史患者、2型多發性內分泌腺瘤病患者等,有胰腺炎病史者慎用。
(三)其他降糖藥物
口服降糖藥物:二甲雙胍、DPP-4i、胰島素促泌劑(磺脲類和格列奈類)、α-糖苷酶抑制劑、噻唑烷二酮類(thiazolidinediones,TZDs),均爲臨床有效的降糖藥物。DKD患者應用時應根據eGFR水平選擇適用的降糖藥物(附錄6)。利格列汀(DPP-4i)、那格列奈(胰島素促泌劑)、羅格列酮和吡格列酮(TZDs)在腎功能不全患者中無需調整劑量,可全程應用。DKD患者服用二甲雙胍期間需監測eGFR變化,eGFR 45~59 ml·min-1·1.73 m-2時應減量,eGFR<45 ml·min-1·1.73 m-2時禁忌使用。CKD G3a期及以下患者在使用造影劑及全身麻醉前需暫停二甲雙胍,完成後48 h複查腎功能無惡化再啓用。
胰島素:由于腎功能不全時腎髒對胰島素清除減少,可導致體內蓄積,胰島素使用過程注意密切監測血糖,及時調整胰島素劑量,避免低血糖發生。
四、降壓治療
DKD患者常伴有高血壓,高血壓加速腎病進展,同時也影響CVD預後。控制高血壓可有效降低DKD患者的尿蛋白水平,延緩腎功能惡化,降低CVD終點事件(如卒中、心肌梗死、CVD相關死亡等)的發生風險。不同腎功能狀態下降壓藥物的使用可參考附錄8。
對于DKD合並高血壓患者,初始降壓治療首選ACEI/ARB類降壓藥,並逐步加量至可耐受的最大安全劑量。ACEI/ARB類降壓藥不僅具有降壓作用,還能夠降低尿蛋白、延緩腎功能下降、改善預後,並且其腎髒保護作用獨立于降壓作用之外。開始應用ACEI/ARB類或劑量增加後2~4周內監測血壓、血肌酐、血鉀水平,如4周內血肌酐升高超過30%,需停藥或減少劑量並尋找急性腎損傷的原因(如腎動脈狹窄);不建議聯合應用ACEI和ARB。出現與ACEI/ARB應用相關的高鉀血症時須停藥,並轉診至上級醫療機構。
使用ACEI/ARB的DKD患者如血壓控制未達標,可在ACEI/ARB的基礎上,聯用鈣通道阻滯劑(calcium channel blocker,CCB)或噻嗪類利尿劑/袢利尿劑(eGFR<30 ml·min-1·1.73 m-2時使用袢利尿劑)。如果兩藥聯合使用血壓未能控制,則推薦使用ACEI/ARB、CCB、利尿劑三藥聯合。在聯合用藥時,推薦單片固定複方制劑(ARB+CCB、ARB/ACEI+利尿劑),固定複方制劑在療效、依從性和安全性方面均優于上述藥物自由聯合。
五、調脂及抗血小板治療
DKD患者的血脂控制目標與調脂治療同一般T2DM患者。但臨床用藥時應根據腎功能水平進行藥物選擇和劑量調整,具體見附錄9。
DKD合並CVD患者在使用抗血小板藥物時應充分評估出血風險,並關注藥物禁忌證。
六、其他DKD獲益藥物
1.非甾體類鹽皮質激素受體拮抗劑非奈利酮:非奈利酮作爲新一代治療藥物,通過阻斷鹽皮質激素受體過度活化而降低T2DM相關且伴白蛋白尿的CKD患者eGFR持續下降、ESRD、心血管死亡和因心力衰竭住院的風險。在T2DM伴白蛋白尿、eGFR≥25 ml·min-1·1.73 m-2、血清鉀濃度≤5.0 mmol/L的患者中,推薦加用對腎髒和心血管有益的非奈利酮。一般起始劑量應爲20 mg,每日1次;eGFR 25~59 ml·min-1·1.73 m-2減量至10 mg,每日1次,具體詳見表5。非奈利酮常見的不良反應爲高鉀血症,因此開始治療、劑量調整的4周內,及整個治療期間需監測血鉀,血鉀>5.5 mmol/L停藥,具體詳見表6。


2.中成藥治療:黃葵膠囊可用于治療DKD,單藥使用時與ARB有相似的降尿蛋白療效,與ARB聯用時能夠在ARB的基礎上進一步降低尿蛋白的水平。另外,以黃芪等中藥組成的糖腎方在ACEI/ARB的基礎上也能進一步降低尿蛋白。
七、基層腹膜透析管理
腹膜透析技術下沉至基層醫療衛生機構可以優化醫療資源配置,方便患者就近就醫,減少時間及經濟成本。基層醫療衛生機構醫務人員應普及腹膜透析相關知識,進行腹膜透析相關的理論及實踐學習,完成腹膜透析專業知識的系統培訓,取得腹膜透析培訓證書,方可進行腹膜透析的相關隨訪工作。同時,還應與上級醫療機構建立良好的互動及轉診策略。即使是在社區隨訪的患者,仍由上級醫院進行患者的全面管理。
患者隨訪
對接受國家基本公共衛生服務項目糖尿病健康管理服務的患者,按照國家有關規範和要求隨訪,每年隨訪不少于4次。隨訪包括以下內容。
1.了解患者症狀、生活方式、輔助檢查結果、血糖控制情況、腎髒損傷情況及其用藥情況。
2.檢測血壓、空腹/餐後血糖,推薦檢測HbA1c。
3.對患者提出運動和合理營養建議。
4.隨訪信息可參照填入“糖尿病腎髒病患者隨訪管理服務記錄表”(附錄10)。
對于糖尿病患者的臨床診療,基層醫療衛生機構參照《國家基層糖尿病防治管理指南(2022)》中有關並發症及合並症的檢查要求執行,每6個月至少開展1次尿常規檢查,每年進行1次血脂、肝腎功能檢測和DKD篩查。
對于已確診DKD患者,應根據CKD分期(G1~G5)和白蛋白尿分期(A1~A3)確定隨訪頻率,以評估疾病進展、指導治療方案調整等(表1)。對于eGFR<60 ml·min-1·1.73 m-2的患者還應監測CKD並發症情況,如貧血、礦物質及骨代謝紊亂等。
轉診
一、建議上轉至二級及以上醫院的情況
(一)篩查困難
無法提供DKD篩查的基層醫療機構,建議向上轉診,完善檢查。
(二)指征明確
已診斷的DKD患者中,UACR>300 mg/g或CKD臨床分期G4、G5期者。
(三)診斷不明
糖尿病患者伴腎髒損害,DKD臨床診斷難以明確時,如出現明顯的鏡下血尿(尿紅細胞≥20個/高倍鏡或尿紅細胞≥80個/μl或尿潛血≥2+)等(具體參照本指南“糖尿病腎髒病篩查、診斷與臨床分期”章節)。
(四)治療複雜
對綜合治療方案的制定、評估、處理有困難者,如血糖、血壓治療長期不達標者,或糖尿病慢性並發症導致嚴重靶器官損害需要緊急救治者。
(五)其他情況
進行腹膜透析的DKD患者至少每3個月需至上級醫院進行規律隨訪1次。另外,出現腹膜透析相關並發症(感染和/或非感染並發症),或心力衰竭、嚴重貧血、電解質及酸堿平衡紊亂等其他社區醫院無法處理者。
二、建議轉回基層醫療衛生機構的情況
經上級醫療機構醫生判定可以轉回基層繼續治療管理的患者。
指南撰寫組名單:賈偉平(上海交通大學醫學院附屬第六人民醫院內分泌代謝科);朱大龍(南京大學醫學院附屬鼓樓醫院內分泌科);蔡淳(上海交通大學醫學院附屬第六人民醫院 國家基本公共衛生服務項目基層糖尿病防治管理辦公室);陳莉明(天津醫科大學朱憲彜紀念醫院內分泌科);陳麗(山東大學齊魯醫院內分泌科);李紅(浙江大學醫學院附屬邵逸夫醫院內分泌代謝科);薛耀明(南方醫科大學南方醫院內分泌代謝科);李啓富(重慶醫科大學附屬第一醫院內分泌科);包玉倩(上海交通大學醫學院附屬第六人民醫院內分泌代謝科);張俊清(北京大學第一醫院內分泌科);徐玉善(昆明醫科大學第一附屬醫院內分泌科);吳天鳳(浙江醫院內分泌科);汪年松(上海交通大學醫學院附屬第六人民醫院腎髒科);居漪(上海市臨床檢驗中心);吳浩(首都醫科大學全科醫學與繼續教育學院);殷峻(上海交通大學醫學院附屬第六人民醫院內分泌代謝科);範瑛(上海交通大學醫學院附屬第六人民醫院腎髒科);宋君(同濟大學附屬東方醫院內分泌科);王月環(江蘇省常州市鍾樓區五星街道社區衛生服務中心);史玲(上海市普陀區衛生健康事務管理中心);勵麗(甯波大學附屬第一醫院內分泌科);葛聲(上海交通大學醫學院附屬第六人民醫院臨床營養科);黃珊(上海交通大學醫學院附屬同仁醫院內分泌科)
起草工作組名單:蔡淳;李紅;包玉倩;殷峻;宋君;範瑛;勵麗;黃珊;彭丹鳳(上海交通大學醫學院附屬第六人民醫院內分泌代謝科);余蓉(上海交通大學醫學院附屬第六人民醫院 上海市糖尿病研究所)
附錄1
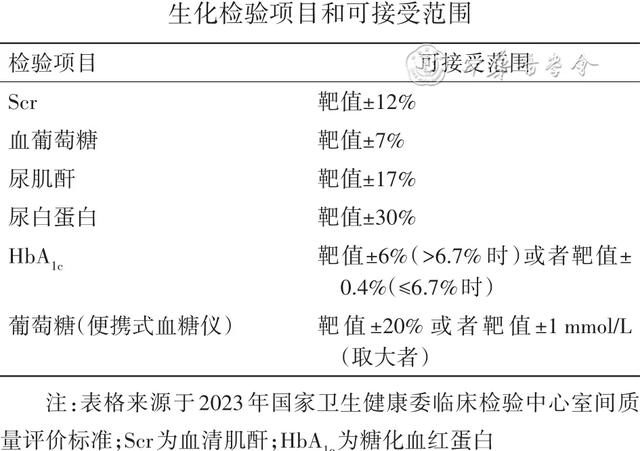
附錄2

附錄3

附錄4 eGFR計算公式
eGFR使用慢性腎髒病流行病學合作研究(CKD-EPI)公式進行計算。eGFR=142×min(SCr/κ,1)α×max(SCr/κ,1)-1.200×0.9938年齡×1.012(如爲女性)(其中SCr爲血清肌酐水平,單位爲mg/dl;κ:女性=0.7,男性=0.9;α:女性=-0.241,男性=-0.302;min爲SCr/κ與1的較小值;max爲SCr/κ與1的較大值)。也可通過網站www.kidney.org/professionals/kdoqi/gfr_calculator進行計算(輸入相應的年齡、性別、血肌酐水平)。
附錄5 目標心率計算公式
最大心率(maximum heart rate,MHR)=220-年齡;目標心率(target heart rate,THR)=(MHR-靜態心率)×(40%~70%)+靜態心率
附錄6 不同腎功能分期降糖藥物的使用

附錄7 降糖藥物綜合獲益、風險評估表

附錄8 不同腎功能分期降壓類藥物的使用

附錄9 不同腎功能分期調脂藥物的使用

附錄10 糖尿病腎髒病患者隨訪管理服務記錄表

注:體征和生活方式指導部分中,斜線前填寫目前情況,斜線後填寫下次隨訪時的目標,其中,運動部分橫線上填寫目前情況,橫線下填寫下次隨訪時的目標;eGFR爲估算的腎小球濾過率;1 mmHg=0.133 kPa
本文編輯:趙景輝